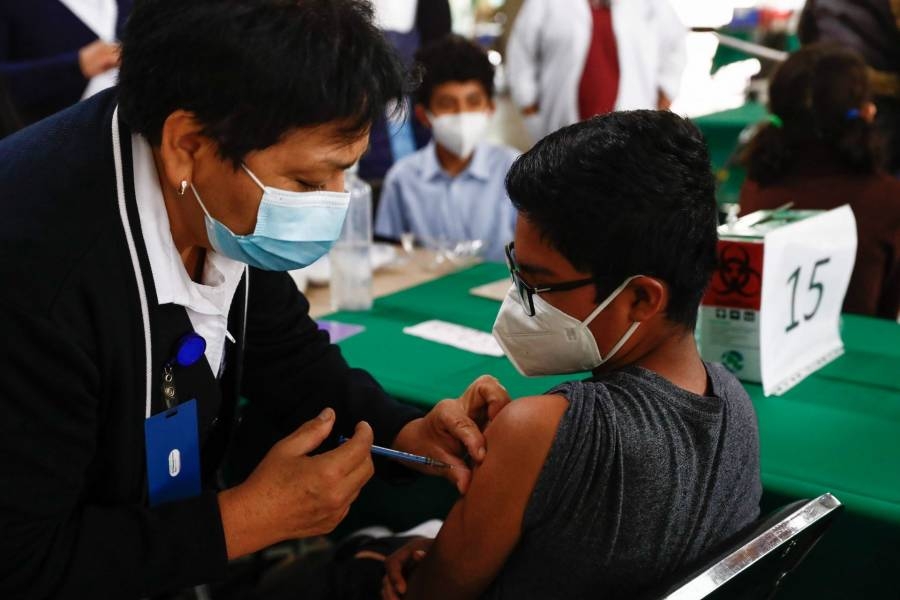
La Agencia Europea de Medicamentos (EMA) comenzó este miércoles a evaluar la posible extensión de la licencia europea de Moderna a niños de entre 6 y 11 años, una vacuna autorizada en la actualidad solo para mayores de 12 años.
El Comité de Medicamentos Humanos de la EMA revisará los datos sobre la vacuna Spikevax, de Moderna, para determinar si respaldan su seguridad y eficacia contra la COVID-19 en esa franja de edad, lo que incluye los resultados de un estudio clínico en curso.

Noticia Destacada
COVID-19 en Quintana Roo: Estas son las colonias con más casos activos en el estado
La agencia espera concluir su evaluación de estos datos en “aproximadamente dos meses” y decidirá si recomendar la extensión del uso de esta vacuna a menores de entre 6 a 11 años, dependiendo de si los datos disponibles son suficientes o se necesitará más información o análisis complementarios.
Las vacunas contra el coronavirus desarrolladas por Moderna y Pfizer-BioNTech ya han sido autorizadas para su uso en jóvenes de 12 a 17 años en el continente europeo, y la mayoría de los países ya están vacunando a los adolescentes.
Pfizer, la vacuna más utilizada en la UE desde su aprobación en diciembre del año pasado, también solicitó a la EMA extender su licencia a niños de 5 a 11 años y la agencia espera concluir la evaluación de los datos presentados por la farmacéutica el próximo diciembre, convirtiendo a esta vacuna en la primera en usarse en esa franja de edad en la UE.
Los países europeos están utilizando en sus campañas de vacunación un total de cuatro vacunas contra el COVID-19: Pfizer/BioNTech, Moderna, AstraZeneca y Janssen, de la estadounidense Johnson & Johnson.
Con información de EFE
Síguenos en Google News y recibe la mejor información
AR