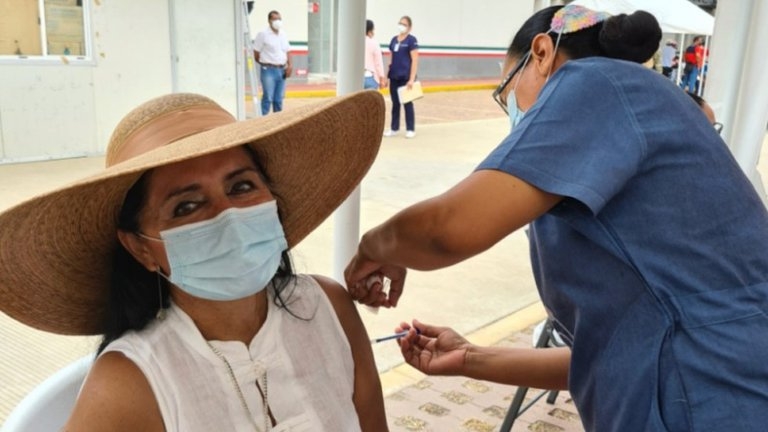
A consecuencia de incumplimiento de requisitos y temor entre los voluntarios, no se logró la meta de las mil vacunas de prueba contra COVID-19 CanSino BIO en Quintana Roo, ya que concluyó el ensayo clínico en la entidad con el suministro de 709 biológicos, sin embargo en Aguascalientes y Oaxaca aumentaron 200 vacunas más en cada estado, es decir se suministraron mil 200 vacunas en cada entidad, dijo Víctor Bohórquez, director de Red Osmo, encargado del ensayo Clínico en estos tres estados.
El director explicó que esto se dio, porque muchos hicieron la cita, para ser voluntarios, continuaron con todo el proceso al final, cuando se llegó la hora de aplicar la vacuna, los participantes se arrepienten, por diversas razones, sin embargo se les respetó su derecho de desistir, hasta el último momento de ser suministrado el biológico.
Otra de las razones, que puede hace más lento el proceso, es que no todos son aptos para esta vacuna, es decir se prefiere, que personas susceptibles a alguno de los componentes de la vacuna, no se les aplique, también los que presentan diversas alergias, esto no porque no se pueda, sólo es un protocolo de precaución.
Mencionó que Oaxaca y Aguascalientes iniciaron la aplicación, algunas semanas antes que en Quintana Roo, sin embargo también se adjudica que mientras en los otros dos estados donde se atendían a 80 participantes al día, en es estado sólo llegaban de 30 a 40 personas.
El monitoreo, será de un año, para los voluntarios que participan en el ensayo de vacuna contra COVID-19 CanSino BIO, además tendrán dos consultas presenciales donde se les tomará una muestra de sangre, un mensaje de texto semanal y 11 llamada telefónicas mensuales, como parte del estudio, en caso de presentan una reacción misma propia de la vacuna el paciente cuenta con un seguro medico en un hospital privado de Cancún, de acuerdo al documento de consentimiento informado que entrega el laboratorio Red Osmo, encargado de la investigación clínica.
Antes de realizar cualquier actividad del estudio, a los voluntarios se les solicitó que revisaran de manera detallada el documento de consentimiento informado y posteriormente lo firmaran, eso le dio al paciente la certeza del entendimiento de la participación y de los posibles riesgos, además de ambas partes estar de acuerdo en cumplir con todo el proceso del estudio clínico.
A los voluntarios se les entregó una copia del mismo documento para que lo conserve, en cada contacto de seguimiento que tengan con los pacientes se reconfirmará verbalmente el deseo de seguir participando.
En la primera visita del estudio, el personal le realizó preguntas sobre su salud, para confirmar si era elegible para la aplicación de la dosis de ensayo, antes de la vacuna se le midió la temperatura corporal, presión arterial frecuencia cardiaca y la frecuencia respiratoria, además de medir altura y peso.
Se tomó muestras de sangre, prueba de embarazo en caso de ser mujer, en caso de ser una persona elegible se le colocó la vacuna o placebo, la vacuna se le aplicó en la visita uno, en el músculo superior y al paciente se monitoreó al paciente un periodo de media hora, para cualquier reacción alérgica inusual.
El voluntario debe de evitar tomar medicamentos de venta libre como paracetamol, ibuprofeno y naproxeno en 12 horas antes de recibir vacuna, sin embargo se le permite tomar estos medicamentos según sea necesario para tratar la fiebre u otros eventos adversos después de la vacunación.
Los requisitos para inscribirse como voluntario fueron ser mayor de 18 años, pudo participar las personas que padecen de alguna enfermedad como diabetes e hipertensión, con la enfermedad controlada, los únicos criterios que se tomaron en cuenta para negar a una persona esta oportunidad es que las mujeres estuvieran embarazada, o en periodo de lactancia y aquellos que ya enfrentaron la enfermedad y cuentan con un examen clínico que lo comprueba positivo.
El director aclaró que la Secretaría de Salud Federal a través de la Comisión Federal para la Protección Contra los Riesgos Sanitarios (Cofepris), autorizó que se lleve a cabo un estudio en el país, los centros de investigación evalúan que estudio se está proponiendo y que el Sponsor, cumpla con toda la normatividad y que cuente con fundamentos científicos y que no se ponga en riesgo las salud de las personas que van a participar, posterior a esto es evaluado por un comité de investigación y seguridad para saber si es viable con la fase uno y fase dos donde se demuestra que no hay ningún problema.
Última fase para el desarrollo de una vacuna
Un ensayo clínico en fase III, es la antesala para que un medicamento salga a la venta al mercado, ya que no puede salir antes realizar ésta última fase y si no cuenta con los permisos de la autoridad regulatoria.
México cuenta con un protocolo clínico que fue aprobado para su ejecución en 20 instituciones de salud, los estados que conforman este grupo, son la Ciudad de México, Jalisco, Chihuahua, Durango, Morelos, Nuevo León, Coahuila, Hidalgo, Aguas Calientes, Oaxaca, Guerrero y Puebla, cabe señalar que Quintana Roo es el único de los tres estados de la península de Yucatán que participó en la aplicación de las vacunas de prueba.
Este ensayo en el que participa México con 15 participantes, es parte de un estudio global en el que serán voluntarios entre 30 y 40 mil voluntarios de países como Chile, Argentina, Pakistán, Arabia Saudita, Rusia y China.
Hugo López-Gatell, a través de sus cuentas oficiales de redes sociales, aclaró que hasta el momento no se ha concedido autorización por parte de la Comisión Federal para la Protección contra Riesgos Sanitarios, a la vacuna de CanSino Biologics para uso de emergencia; ya que todavía no ha presentado el expediente completo.
La directora de Epic Research y responsable del ensayo clínico de la vacuna CanSino en México, dio a conocer que todas las vacunas tienen un proceso regulatorio, estricto y de verificación de datos de seguridad y de eficacia, es por ello que se presentó la solicitud, para su uso de emergencia en la Comisión Federal para la Protección de Riesgos Sanitarios (Cofepris) como todas las compañías, sin embargo está vacuna se encuentra en proceso de evaluación.
Explicó que es un biológico muy noble, cuenta con un control de temperatura entre dos y ocho grados centígrados, es por ello que es manejable y de mayor practicidad a la hora de distribuirlas, además que sólo se requiere una dosis, para lograr su efectividad, la fase uno y dos han les ha indicado que con una aplicación es suficiente, para lograr una eficacia necesaria. También dijo que de las 15 mil dosis de CanSino BIO destinadas para México, se han aplicado más de 12 mil.
CI